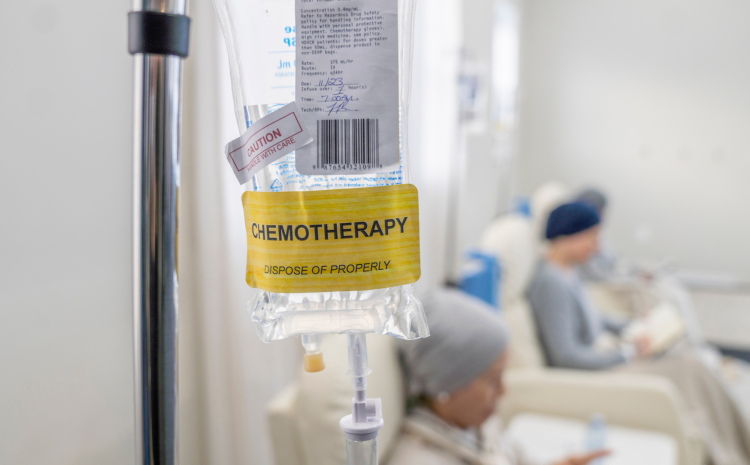
L’administration des traitements anticancéreux est une étape cruciale qui requiert compétence, rigueur et souci du détail. L’infirmier doit s’assurer que le bon médicament est administré au bon patient, à la bonne dose, par la bonne voie et au bon moment.
Des contrôles à plusieurs niveaux sont généralement mis en place pour éviter les erreurs, souvent avec des vérifications à double ou triple niveau entre plusieurs membres du personnel soignant.
En outre, le patient lui-même est souvent impliqué dans ce contrôle pour confirmer son identité et le traitement qu’il est sur le point de recevoir.
Des équipements technologiques comme les lecteurs de code-barres peuvent également être utilisés pour minimiser les erreurs humaines.
Après l’administration, une surveillance étroite est nécessaire pour identifier et gérer rapidement tout effet secondaire ou complication qui pourrait survenir. Ce suivi est essentiel pour ajuster les doses futures ou apporter des modifications au plan de traitement, si nécessaire.